Por: I.A. Stalin Revelo
Jefe de investigación y desarrollo
La acumulación de sales en la zona radical tiene un impacto negativo directo en el crecimiento y la calidad de los tallos exportables, reduciendo la capacidad de la planta para absorber agua y nutrientes y causando un desbalance iónico, especialmente en los cloroplastos de las hojas, lo que reduce la fotosíntesis (Cabrera, 2011). Sin embargo, en la mayoría de los casos, atribuimos los efectos dañinos de las concentraciones de sales únicamente al catión sodio (Na+) e ignoramos al anión cloro (Cl–), aunque esto no debería ser así, ya que la toxicidad por Cl– es una parte importante de los efectos del estrés salino en las plantas (Estebez, 2019).
La acumulación de cloro en los tejidos de las plantas, especialmente en las raíces, puede disminuir significativamente la absorción de nitrato (Taiz et al., 2021) debido a que el flujo activo de Cl y NO3 dentro de la célula es catalizado por las mismas proteínas transportadoras, lo que facilita su movimiento entre células del tonoplasto y llegar a los brotes nuevos (Azcon et al.,2000).
El Cl– al igual que el Na+, por acumulación, puede llegar a ser tóxico para las plantas. Se ha demostrado que la acumulación de Cl- en las hojas está correlacionada con la reducción en la respiración, la tasa de fotosíntesis y, por ende, el rendimiento (Coll et al., 2019).
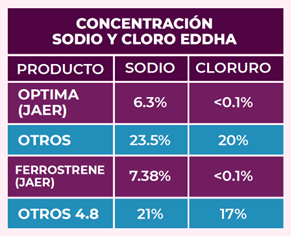
Por lo tanto, una de las características más importantes a tomar en cuenta, en el momento de elegir un quelato, es determinar la cantidad de elementos perjudiciales que contiene el producto, como lo son: sodio (Na) y cloro (Cl), que vienen dentro de los quelatos EDDHA (Cuadro 1).
Los quelatos de hierro Fe-EDDHA Óptima y Ferrostrene de JAER tienen baja concentración de sodio, 6,3 y 7,38%, respectivamente y están libres de cloro. Los quelatos de hierro del mercado llegan a 23% de concentración de sodio y 20 % de concentración de cloro, con lo cual se inyecta al sistema sales nocivas que aumentan la salinidad de manera importante.
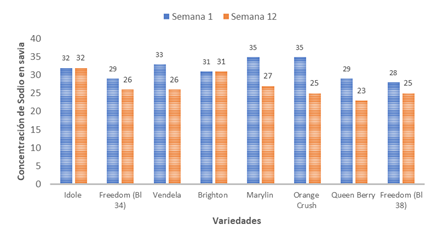
La apariencia visual y estética de las flores se ve muchas veces afectada por los efectos negativos de la salinidad, que son características cruciales para el valor comercial de las especies ornamentales (Flores, 2011) provocando reducciones en la productividad y en la calidad de tallos exportables. En un ensayo realizado con quelato Fe-EDDHA Óptima en una finca en Cayambe (Figura 1), se pudo determinar la disminución de sodio (Na) a nivel de savia en pedúnculo, desde la semana 1 (inicio del ensayo) a la semana 12 (finalización). Se observa que las concentraciones de sodio (Na) decrecieron significativamente, pasando de tener un promedio de 31,5 ppm al inicio del ensayo en semana 1, a concentrar 26,8 ppm en la semana 12 de la aplicación de los quelatos, mejorando la calidad de la flor y reduciendo el amarillamiento en hoja vieja. Además, en variedades como Marylin y Orange Crush, la reducción de sodio fue mayor a 10 ppm.
En el mismo ensayo se registraron los valores de índice de clorofila (IC) que se presentan en la Figura 2, donde se observa que al inicio del ensayo, en la semana 1, el promedio de índice de clorofila era de 53,54 unidades de clorofila; para la semana 12 del experimento se observa un crecimiento en el promedio de índice de clorofila, llegando a 56,41. La variedad que más creció pasó de un índice de 48,5 a 58 unidades de clorofila, mejorando el verdor y el brillo de las hojas; posiblemente, también aumentó la cantidad de fotoasimilados.

La aplicación de quelatos Fe-EDDHA sin contaminantes como sodio (Na) y cloro (Cl) mejoraron la calidad de los tallos evaluados, disminuyendo el contenido de sodio en savia y, por otra parte, aumentando el índice de clorofila (IC) en hojas, lo que conlleva un aumento en la tasa fotosintética y la cantidad de fotoasimilados. Por otra parte, mejora la Conductividad Eléctrica (CE) del sistema, tanto en suelo como en planta, dando mayor oportunidad al ingreso de nutrientes esenciales como potasio y calcio al sistema. Una ventaja los quelatos ADOB® EDTA (MnK 2 EDTA-12,5%, ZnK 2 EDTA – 14,5% y Cu(NH 4 ) 2 EDTA – 15,5%) es que son libres de sodio (Na), y a su vez, este elemento ha sido reemplazado por potasio (K), disponible para las plantas, lo que es especialmente importante en cultivos con susceptibilidad a la acumulación de sales como son los ornamentales.
Bibliografía
- Azcón, J. y M. Talón. 2000. Fundamentos de fisiología vegetal. McGraw Hill Interamericana, Barcelona. 656 p.
- Adiloğlu, S. (2021). Relation of chelated iron (EDDHA-Fe) applications with iron accumulation and some plant nutrient elements in basil (Ocimum Basilicum L.). Polish Journal of Environmental Studies.
- Álvarez-Fernández, A., Garcıa-Marco, S., & Lucena, J. J. (2005). Evaluation of synthetic iron (III)-chelates (EDDHA/Fe3+, EDDHMA/Fe3+ and the novel EDDHSA/Fe3+) to correct iron chlorosis. European Journal of Agronomy, 22(2), 119-130.
- Coll, J. B., Rodrigo, G. N., García, B. S., & Tamés, R. S. (2019). Fisiología vegetal. Comercial Grupo ANAYA, SA.
- Calvache Ulloa, M. (2008). Fertirriego en Ecuador, Presente y Futuro. X Congreso Ecuatoriano de la Ciencia del Suelo.
- Estévez, M. M. (2019). Cloro… el enemigo olvidado…¿ o no?. Desde El Herbario CICY, 11, 240–243, 2019.
- Flórez, V. J. Avances sobre fisiología de la producción de flores de corte en Colombia.
- Hernández-Apaolaza, L., Barak, P., & Lucena, J. J. (1997). Chromatographic determination of commercial Fe (III) chelates of ethylenediaminetetraacetic acid, ethylenediaminedi (o-hydroxyphenylacetic) acid and ethylenediaminedi (o-hydroxy-p-methylphenylacetic) acid. Journal of Chromatography A, 789(1-2), 453-460.
- Lucena, J. J. (2000). Effects of bicarbonate, nitrate and other environmental factors on iron deficiency chlorosis. A review. Journal of Plant Nutrition, 23(11-12), 1591-1606.
- Lucena, J. J. (2009). El empleo de complejantes y quelatos en la fertilización de micronutrientes. Revista Ceres, 56(4), 527-535.
- Moreno Lora, A. (2023). Efecto de las propiedades del suelo, la materia orgánica y la actividad microbiana sobre la biodisponibilidad de zinc y otros micronutrientes y su interacción con el fósforo.
- Taiz, L., Zeiger, E., Møller, I. M., & Murphy, A. (2021). Fundamentos de Fisiologia Vegetal-6. Artmed Editora.
- Zuluaga, M. Y. A., Cardarelli, M., Rouphael, Y., Cesco, S., Pii, Y., & Colla, G. (2023). Iron nutrition in agriculture: From synthetic chelates to biochelates. Scientia Horticulturae, 312, 111833.








